深度解读|2026版《医疗器械生产质量管理规范》新旧对比
核心变化:从10章增至15章,条款从约80条增至132条
2025年11月4日,国家药监局发布新版《医疗器械生产质量管理规范》(以下简称“新版《规范》”),将于2026年11月1日起正式施行。这是自2014年旧版发布以来的一次重大修订。英硕医用包装第一时间组织学习,现将核心变化梳理如下,供行业同仁参考。
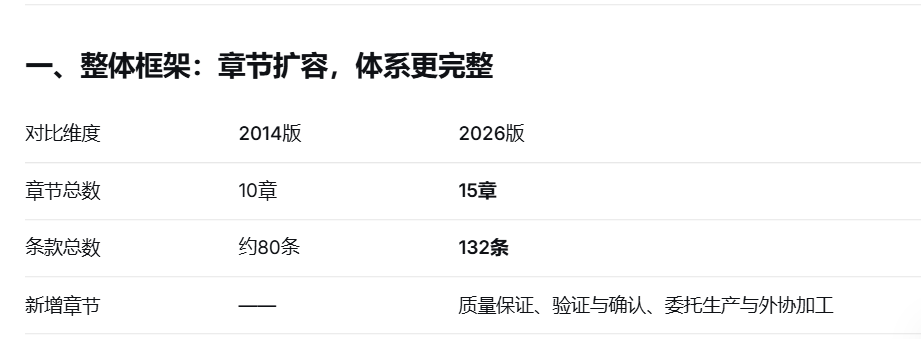
新版《规范》在保留机构与人员、厂房与设施、设备、文件管理、设计开发、采购、生产管理、质量控制、销售与售后服务、不合格品控制等核心章节的基础上,新增三个独立章节,使质量管理体系覆盖产品全生命周期。
二、三新增章节解读
1. 质量保证
核心要求:
建立覆盖产品全生命周期的质量保证体系
规范管理评审与内部审核
将不良事件监测、数据分析、持续改进纳入体系闭环
解读:从“质量控制”向“质量保证”转变,强调事前预防与持续改进。英硕医用包装已建立完善的质量保证体系,并通过ISO 13485:2016认证,为持续合规奠定基础。
2. 验证与确认
核心要求:
明确工艺验证、灭菌验证、包装验证等关键环节
强调验证状态的持续保持与再验证
建立验证主计划与验证方案管理
解读:验证与确认从“附属要求”变为“独立章节”,体现了对过程有效性的高度重视。作为医用吸塑包装企业,英硕医用包装在密封性能验证、灭菌适应性验证等方面持续投入,确保包装系统符合无菌屏障要求。
3. 委托生产与外协加工
核心要求:
将委托生产、外协加工纳入质量管理体系
明确注册人主体责任与受托方职责划分
建立供应商动态管理机制
解读:结合医疗器械注册人制度,进一步压实委托生产中的质量责任。英硕医用包装作为配套供应商,将持续优化供方管理体系,与客户共同保障质量安全。
三、重点条款修订要点
1. 设计开发
主要变化:
风险管理贯穿设计开发全过程
细化设计转换、设计确认、设计变更要求
强调设计与生产的衔接
2. 采购与物流管理
主要变化:
强化供应商分类管理与动态评价
明确关键物料追溯性要求
增加外协加工质量管控
3. 生产管理
主要变化:
细化环境控制与洁净区管理要求
强化批生产记录完整性与可追溯性
明确过程控制与工艺参数管理
4. 质量控制
主要变化:
规范放行审核程序与责任
细化检验记录管理要求
强调不合格品控制与纠正预防措施
四、核心导向:三个转变

五、给行业同仁建议
距离2026年11月1日实施尚有过渡期,建议相关企业:
1. 开展差距分析
对照新版132条要求,逐条评估现有体系的符合性。
2. 完善三大新增板块
重点关注质量保证、验证与确认、委托生产三个新增章节的要求落地。
3. 强化关键岗位培训
组织质量负责人、生产负责人、管理者代表等关键岗位人员系统学习。
4. 提前自查整改
在过渡期内完成体系优化,确保按时符合新版要求。
结语
新版《规范》的实施,是推动医疗器械产业高质量发展的重要举措。英硕医用包装始终秉持“质量与服务为灵魂”的企业理念,拥有万级洁净车间、ISO 13485:2016体系认证,专注于为医疗器械行业提供安全、可靠的吸塑包装解决方案。我们将持续关注法规动态,与行业同仁一道,共同守护医疗器械质量安全防线。
——责任编辑:英硕包装
版权所有//m.ludgerpistor.com转载请注明出处
相关推荐:
最新产品
同类文章排行
- 《无菌医疗器械包装:标准体系与检测项目全解读》
- 重磅解读 | 医疗器械初包装微粒污染怎么测?新国标来了!附英硕包装实战经验
- 2026无菌医疗器械常用包装材料与包装形式灭菌方式指南
- 深度解读|2026版《医疗器械生产质量管理规范》新旧对比
- 影响环氧乙烷灭菌效果的因素
- 无菌包装材料的评估项目及测试方法参考
- 影响医疗器械货架有效期的因素
- 《医疗器械初包装的生产环境要求》
- 《最终灭菌医疗器械包装合规标准参考》
- 疫情期间,医用吸塑托盘整柜发往国外
最新资讯文章
您的浏览历史










 粤ICP备14050553号-1
粤ICP备14050553号-1